近日,首發展投資企業北(běi)京中(zhōng)因科技有限公司(以下(xià)簡稱中(zhōng)因科技)宣布,美國食品和藥品監督管理局(FDA)授予公司眼科基因治療産品ZVS203e-1孤兒藥資格認定(ODD)。這是繼ZVS101e之後,獲得的第二個FDA授予的孤兒藥資格認定。
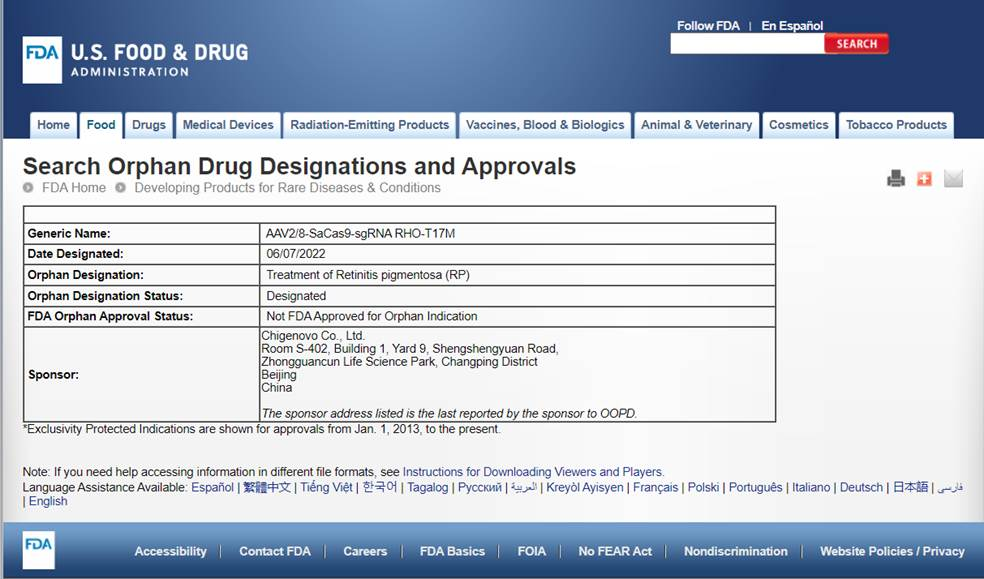
FDA在其官網進行了相關公示
ZVS203e-1注射液是由中(zhōng)因科技自主研發,用于治療視網膜色素變性(RP)的基因編輯治療産品。目前該項目已完成主要非臨床研究工(gōng)作,結果顯示良好的安全性及顯著有效性。
RP是一(yī)種以感光細胞和色素上皮細胞進行性、選擇性喪失爲特點的進展性單基因緻盲眼病,中(zhōng)國人群患病率爲1/1000。RP臨床表現最初是夜盲,大(dà)多數患者兒童期或青少年期發病,随着病情進展,視野逐漸縮小(xiǎo)伴中(zhōng)心視力逐漸下(xià)降,患者于20-65歲之間即發展爲法定盲人。目前已知(zhī),近80個基因的突變與RP發病相關,RHO(Rhodopsin,視紫紅質)基因是最爲常見的常染色體顯性遺傳RP(adRP)緻病基因,占adRP的25-30%。ZVS203e-1注射液拟針對RHO基因特定位點進行編輯治療,此适應症目前尚無任何有效療法。
ZVS203e-1獲得FDA孤兒藥認證,再次證明了中(zhōng)因科技在眼科疾病基因治療産品的早期概念驗證、産品開發方面具有豐富的人才儲備和技術積累。未來公司仍将持續專注于眼科基因治療産品多管線的開發,以期爲眼科疾病的基因治療帶來更多的可能。
孤兒藥認定(Orphan Drug Designation, ODD)是FDA 孤兒藥産品開發辦公室(Office of Orphan Products Development, OOPD)對符合條件的用于預防、治療及診斷罕見病的藥物(wù)(包括生(shēng)物(wù)制品)授予的一(yī)種資格認定。根據美國《孤兒藥法案》,凡獲得孤兒藥資格認定的新藥,将有機會獲得美國7年市場獨占權、稅費優惠、快速審批通道等一(yī)系列配套權益。

北(běi)京中(zhōng)因科技有限公司是一(yī)家專業從事遺傳性眼病臨床基因診斷、生(shēng)育預防和基因治療藥物(wù)研發的國家高新技術企業,緻力于爲遺傳性眼病患者提供診療全程“一(yī)站式”服務。公司基因治療平台基于基因替代和基因編輯治療兩個方向建立了從靶标篩選、基礎研究、動物(wù)實驗、幹細胞驗證到AAV病毒生(shēng)産完整的藥物(wù)開發體系,在國内率先進行了眼科基因治療藥物(wù)研發,探索性臨床試驗表現出了優異的療效和安全性。公司基因診斷平台聚焦眼科遺傳病精準診斷、生(shēng)育預防和大(dà)衆視力健康,擁有第三方醫學檢驗機構資質,可爲遺傳性眼病患者提供快速、準确、可靠、專業的基因檢測與遺傳咨詢服務。

中(zhōng)因科技爲首發展下(xià)屬基金首科開陽投資企業,在首科開陽投資後,集團聯合北(běi)京市科技金融促進會、北(běi)京市創業孵化協會爲投後項目舉辦專場路演等活動,多次爲中(zhōng)因科技提供資本對接機會和渠道。
來源:中(zhōng)因科技